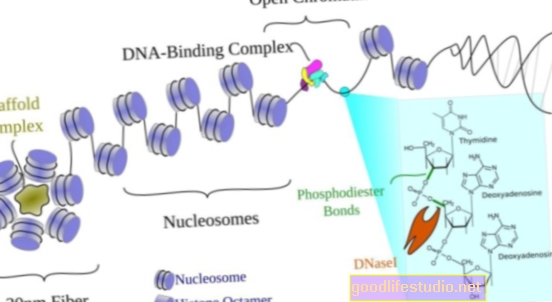
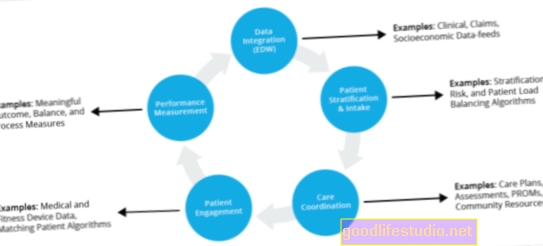
人工椎間板:腰の本当の再建手術
これは腰痛に苦しむ患者にとって非常に刺激的な時期です。 最後に、脊椎手術は、30年以上にわたって行われている関節置換手術の残りに追いついています。 現在、脊椎手術は「サルベージ」手術から実際の再建手術に移行しています。
人工椎間板置換は現在2つの食品医薬品局(FDA)の研究で研究されており、患者に新しい選択肢を提供しています。 過去には、椎間板変性症の患者または過去に椎間板ヘルニア手術を受けた患者を治療するための唯一の外科的選択肢が融合でした。 現在、人工椎間板置換を含む代替手段があります。
新しい概念ではない
人工椎間板置換の概念は新しいものではありません。 1987年にはヨーロッパでLink®SBCharitéIIIが導入されました。 これまでに世界中で4, 000人以上の患者がこの人工椎間板を受け取っています。 1990年代初頭、テキサスバック研究所はLink®Spine Group、Inc.と協力して、FDA承認申請の完了を支援しました。

CHARITÃ人工椎間板(DePuy Spine、Inc.)
写真提供:DePuy Spine、Inc.
食品医薬品局(FDA)は、変性椎間板疾患に伴う疼痛の治療に使用するために、CHARITÃ人工椎間板(マサチューセッツ州レイナムのDePuy Spine、Inc.)を承認しました。 このデバイスは、少なくとも6か月間の非外科的治療後に腰痛が緩和されていない患者に対して、腰椎の1つのレベル(L4-S1から)での使用が承認されました。
Link®SBCharité人工椎間板のさらなる生体力学的研究を実施し、その有効性と機械的摩耗に耐える能力を確認しました。 2000年3月、最初の患者はFDAの調査の下、テキサスバック研究所でCharité椎間板移植を受けました。 それ以来、私たちの研究所は、米国の14の調査センターの中で主要な調査サイトであり続けています。
フェーズ1
FDA研究の第1フェーズは2001年12月に完了し、291人の患者が登録されました。 これらの患者の3分の2がLink®人工椎間板を受け取りました。 これらの患者は2年間厳密に追跡され、情報はFDAに提出されます。 これまでのところ、結果は十分に有望であり、2002年半ばまでに、ランダム化されないSBシャリテ人工椎間板研究の第2段階が開始されることを願っています。
PRODISC®:人工椎間板の一種
PRODISC®は、FDAの調査で現在調査中の2番目の人工椎間板です。 1990年代初頭、フランスの外科医であるThierry Marnay博士はPRODISC®を開発しました。 2001年10月、最初のPRODISC®が、米国の約10の調査サイトの主要調査サイトであるテキサスバック研究所に移植されました。

PRODISC®(Spine Solutions、ニューヨーク、ニューヨーク、米国)
食品医薬品局(FDA)は、PRODISC®-LTotal Disc Replacement(ペンシルベニア州ウエストチェスターのSynthes Spine、Inc.)を承認しました。 この人工椎間板は、骨格的に成熟しており、腰椎に1つのレベルで変性椎間板疾患(DDD)があり(L3-S1から)、関与するレベルでグレード1の脊椎すべり症を患っており、少なくとも6か月間の非外科的治療後の痛みの緩和はありません。
現在までに、約70人の患者がPRODISC®プロテーゼの移植を受けています。 一部の患者はほぼ正常な活動に戻っており、良好から優れた結果が得られています。 米国でのこの製品の一般的な入手可能性は、少なくとも2年先のFDA調査の結果待ちです。
結論
最初の結果は肯定的なようであり、人工椎間板は、非外科的治療に反応しなかった慢性腰痛に苦しむ患者にとって画期的なものであることが証明されるかもしれません。 今後2年以内に、人工椎間板の移植を開始できるようになることを期待しています。