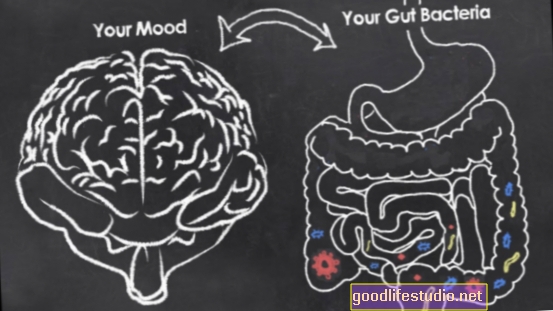
マウス研究は不安への遺伝的手がかりを明らかにします
シカゴ大学の研究者たちは、不安やその他の精神疾患の新しい治療法につながる可能性のある代謝副産物と脳活動との関連を明らかにしました。
不安におけるGlo1と呼ばれる遺伝子の役割をテストしている間に、科学者たちは脳の新しい抑制因子である代謝副産物メチルグリオキサール(MG)を発見しました。この研究は、 Journal of Clinical Investigationシカゴ大学医学部の人間遺伝学助教授であり、研究の筆頭著者でもあるAbraham Palmer博士は、Glo1遺伝子の複数のコピーを持つ動物は、実験室試験で不安のような行動を示す可能性が高いことを発見しました。 。
「Glo1は単に相関するのではなく、因果的に不安のような行動に関連していることを示しました」と彼は言った。
さらなる実験は、Glo1がMGのレベルを下げることによって不安のような行動を増加させることを示しました。研究者がGlo1を阻害したり、MGレベルを上げたりすると、不安行動が減少しました。
2005年、さまざまなマウス系統を比較すると、不安様行動と代謝酵素グリオキシラーゼ1をコードする遺伝子であるGlo1との間に関連性があることが判明しました。しかし、その後の研究では、関連性、およびグリオキシラーゼ1と脳機能との明らかな関連性の欠如が疑われました研究者によると、行動によって一部の科学者は懐疑的になったという。
「人々が遺伝子を発見するとき、彼らが彼らがすでに知っている何かを発見するとき、彼らは常に最も快適です」とパーマーは言いました。 「ここでの憂慮すべきことは、誰も知らない何かの発見があったため、実際に正しい可能性は低いように思われました。」
パーマーの研究室での2009年の研究では、マウス系統間のGlo1発現の違いは、遺伝子を含むゲノムのセグメントが複数回繰り返されるコピー数変異によるものであることが示唆されました。この仮説を検証するために、筆頭著者のマーガレット・ディスラーは、Glo1遺伝子の2、8、または10コピーをマウス系統に挿入しました。その後、研究者は不安の変化を検出するために、マウスがアリーナの中心と壁に沿って費やす時間を測定するオープンフィールドテストなどの実験を行いました。
その結果、Glo1遺伝子のコピー数が多いマウスほど、不安に似た行動を示すことが確認されました。
「これは、Glo1の発現と振る舞いを変える可能性があるのはコピー数多型であることを示した最初の研究です」とM.D./Ph.DのDistler氏は述べています。プリツカー医学部の医学科学者トレーニングプログラムの学生。
その後、研究者たちは、Glo1が不安のような行動にどのように影響するかという謎を解き始めました。 Glo1の主な機能は、解糖の廃棄物であるMGの代謝と細胞レベルの低下です。 Distlerは、MGを注射して脳内のそのレベルを人工的に増加させることにより、反対の効果を生み出しました。MGレベルを上げると、マウスの不安症状がすぐに減少することがわかりました。
「メチルグリオキサールは、投与後10分以内に行動を変化させました。つまり、急速に発症します。遺伝子発現に変化はなく、長期的な下流への影響もありません」と、ディストラー氏は語った。 「それが私たちの最初の進歩でした。」
MGはニューロン活動に直接影響を与える可能性があることを短時間で示唆した、と彼女は言った。 MGはまた、高用量で鎮静効果を示した、これはニューロンの抑制性GABA受容体を活性化する薬物の特徴であると研究者らは付け加えた。現在ブランダイス大学にいるリープラント博士と共同で、研究者たちは、MGがニューロンのGABA-A受容体を活性化することを実証しました。
「それは、神経抑制トーンを代謝活動に結びつける完全に異なるシステムです」とパーマーは言いました。 「解糖系が進化して以来ずっと存在していたメチルグリオキサールもこれらの受容体に作用していたことがわかりました、そして誰もそれを知りませんでした。」
不安は通常、ベンゾジアゼピンやバルビツール酸塩などのGABA-A受容体を活性化する薬物で治療されます。ベンゾジアゼピンや乱用は危険な副作用を起こしやすい傾向があります。研究者たちは、Glo1 / MGの相互作用をターゲットにすることで、抑制トーンに微妙に影響を与えることで、不安を軽減するためのより選択的な戦略を提供できると理論づけました。
「GABA-A受容体はすでに存在しており、鎮静作用や低体温症などの多くの副作用があり、乱用の可能性が高い」とDistler氏は述べた。 「Glo1阻害剤を服用すると、MGレベルのみが特定の最大値に上昇する可能性があります。メチルグリオキサールやその他のGABA-A受容体物質を脳全体に放出するだけでなく、すでに導入されているシステムをアクティブ化している場合、より特異性が高まる可能性があります。」
Glo1の小分子阻害剤を用いた予備実験がこの理論を裏付けました。希望の都市のベックマン研究所のジョンテルミニによって開発された阻害剤の注射は、マウスの不安のような症状を軽減しました。
「これは、これらのGABA-A受容体を攻撃する別の方法です」とパーマー氏は語った。 「それがより良い方法であるかどうかはまだ判断していませんが、それは確かに異なり、このシステムに対する独自の攻撃角度と、まだ評価していない潜在的な利点をもたらします。」
そのような薬剤はまた、てんかんや睡眠障害の治療にも有用である可能性があり、GABA-A薬剤は成功を収めていると彼は付け加えた。
治療の可能性はまだ決定されていないが、研究は行動と細胞の証拠を追加することによって不安におけるGlo1の役割の周りの霧をクリアすると研究者は指摘している。
「すばらしいのは、マウスを用いた探索的で制限のない遺伝子研究から始めたことで、これまで誰も評価したりまとめたりしていない、いくつかの根本的な新しい生理学に到達したことです」とパーマー氏は語った。 「私たちは今、生物学のより古典的な側面についての理解を深めるために、これらのタイプの遺伝子研究からいくつかの実を収穫し始めています。」
出典:シカゴ大学医療センター