抗精神病薬は監視する必要があります
研究者たちは、薬の使用に伴う糖尿病のリスクに関する警告にもかかわらず、これらの薬で治療されているメディケイド患者の3分の1未満が潜在的な糖尿病のスクリーニングを受けることを発見しました。
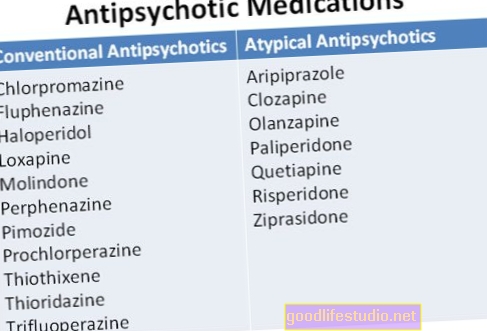
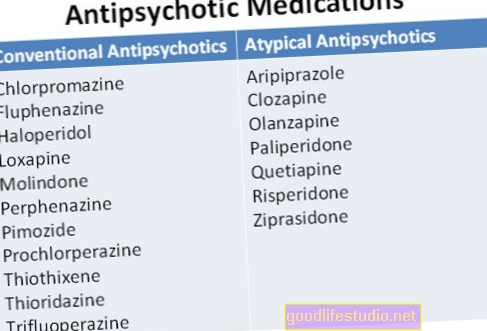
2003年に、食品医薬品局(FDA)は、高血糖と糖尿病のリスクの増加を説明する、オランザピン(ジプレキサ)、アリピプラゾール(アビリファイ)、リスペリドン(リスパーダル)などの第2世代の抗精神病薬のラベルに関する警告を要求し始めました。記事の背景情報によると。
この警告は、糖尿病の患者、疾患のリスクがある患者、または高血糖の症状がある患者では、グルコースレベルを監視する必要があると述べています。同時に、アメリカ糖尿病協会とアメリカ精神医学会は、第2世代の抗精神病薬に関連する代謝リスクを説明し、これらの薬物療法を受けるすべての患者のモニタリングプロトコルを指定する合意声明を発表しました。
コロラド大学デンバー校のElaine H. Morrato、Dr.PH、MPH、および同僚は、2002年から2005年の間に、3つの州(カリフォルニア、ミズーリ、オレゴン)のメディケイド集団からの臨床検査データを調査しました。代謝検査(血液検査)第2世代の抗精神病薬を投与された109,451人の患者のグループと、抗精神病薬ではなくアルブテロール(喘息薬)の服用を開始した203,527人の対照グループとの間で、グルコースと脂質のレベルを比較しました。
FDAの警告の前後で料金も比較されました。
第二世代抗精神病薬で治療された患者の初期検査率は低く、27%がグルコース検査を受け、10%が脂質検査を受けました。 FDAの警告は、グルコース検査の増加とは関係なく、脂質検査率のわずかな増加(1.7パーセント)にのみ関連していました。
「第2世代の抗精神病薬で治療された患者の検査率と傾向は、アルブテロール対照群で観察されたバックグラウンド率と変わらなかった」と著者らは書いている。
代謝リスクが高いオランザピンの新しい処方は、警告期間中に減少しました。低リスクの薬物アリピプラゾールの処方数は増加しましたが、これは、同じ期間中にカリフォルニア州で薬物の事前承認が削除されたことが原因である可能性もあります。
「この遡及的研究では、FDAの警告後に検査室スクリーニングが増加しなかった理由を特定または定量化できなかったが、処方慣行は変更されたが、いくつかの可能な説明について推測する可能性がある」と著者らは記している。
リスクの低い薬に切り替えるか、薬の治療を完全に回避することは、新しいスクリーニング手順を開始するよりも簡単な場合があります。さらに、調査は精神科医がこれらの薬物の代謝リスク因子を認識していることを示していますが、必要な臨床検査を一般的に注文するプライマリケアプロバイダーはそうではないかもしれません。
「第2世代の抗精神病薬を投与された患者が糖尿病と脂質異常症についてスクリーニングされ、患者の適切な予防的ケアと治療を受けることができるように、血清グルコースと脂質のベースラインテストから始めて、潜在的な薬物の影響を確実に監視するためにより多くの努力が必要です。 」と著者らは結論付けている。
レポートは、1月号に掲載されています。 一般精神医学のアーカイブ、JAMA / Archivesジャーナルの1つ。
出典:JAMA and Archives Journals